Die Implantate der PROPEL-Produktfamilie: ein neuer Baustein der Versorgung
Die PROPEL-Produktfamilie umfasst 3 steroid-freisetzende Implantate einer Marke, sodass HNO-Ärzte die den anatomischen Gegebenheiten ihrer Patienten am besten entsprechende Option wählen können.1,2

Verbessern Sie Ihren Nebenhöhlenoperationsplan mit den Implantaten der PROPEL-Produktfamilie, einer Innovation der Sinustechnologie
Die PROPEL-Implantate besitzen einen innovativen 2-in-1-Mechanismus; sie öffnen die Nebenhöhlen und geben gleichzeitig Mometasonfuroat, ein starkes Kortikosteroid für die Nebenhöhlenschleimhaut, genau dort ab, wo es gebraucht wird.1,2
ÖFFNET die Nasennebenhöhle
- Selbstexpandierendes Design zur Öffnung und Stabilisierung der Nasennebenhöhle1
- Nicht-obstruktives Design zur Nasenentleerung und Zuführung von topischen Spülungen1
- Auflösbarer Rahmen über ca. 30 bis 45 Tage hinweg nach der Implantation im Zuge der Heilung der Nasennebenhöhle14
SETZT lokal Mometasonfuroat (MF) FREI
- Setzt 370 µg MF über 30 Tage hinweg frei
- MF ist in der Schleimhaut bis zu 60 Tage lang nachweisbar5 (auf Grundlage von präklinischen Daten)

MF bietet die ideale Kombination aus Wirkstärke und Sicherheit
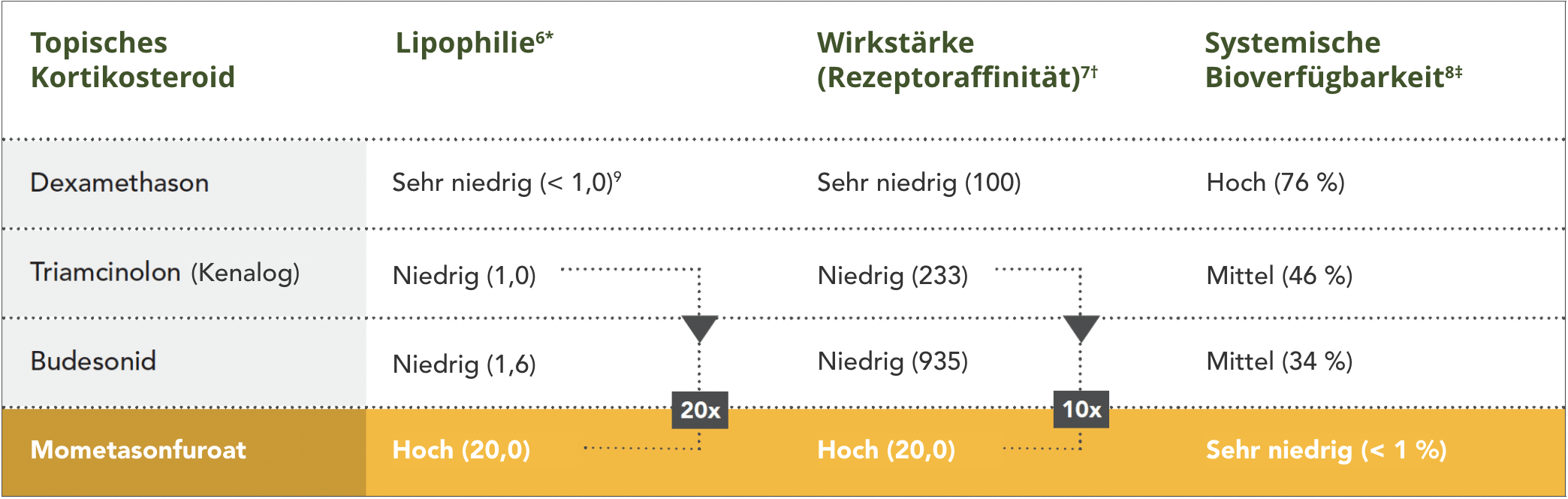
* Die Werte zur Lipophilie sind relativ zu Triamcinolonacetonid normalisiert.
† Gemessen an der relativen Rezeptorbindungsaffinität im Vergleich zu Dexamethason, für die ein Wert von 100 angesetzt wird. Höhere Werte bedeuten eine höhere Wirkstärke.
‡ Gemessen an der Plasmakonzentration des Medikaments bei intranasaler gegenüber intravenöser Verabreichung.
PROPEL-Implantate halten klinisch belegt die Durchgängigkeit aufrecht und setzen Mometasonfuroat lokal in der Nebenhöhlenschleimhaut frei
- PROPEL ist das einzige Produkt für die Nebenhöhlenchirurgie mit Evidenz der Stufe 1a11
- 35%ige relative VerringerungII der Notwendigkeit einer postoperativen Intervention11
- Bessere Auswahlmöglichkeiten für Ärzte: kleine Größe, einzigartige Sanduhrform, flexibler Applikator
- 65%ige relative VerringerungII von postoperativen Interventionen12–13

* Bei der postoperativen Intervention handelt es sich um eine Kombination aus der Notwendigkeit chirurgischer Interventionen, um Vernarbungen zu trennen, und/oder der Notwendigkeit, orale Steroide zur Behandlung von Entzündungen zu verschreiben.
† Beurteilt durch einen unabhängigen Gutachter oder ein unabhängiges Gremium.
‡ Beurteilt durch klinische Prüfärzte.
§ Sekundäre Endpunkte wurden nicht an die Multiplizität angepasst.
| p-Werte wurden an die Multiplizität angepasst.
|| Alle relativen Verringerungen als (T-C)/C als Teil der Ad-hoc-Analyse berechnet.
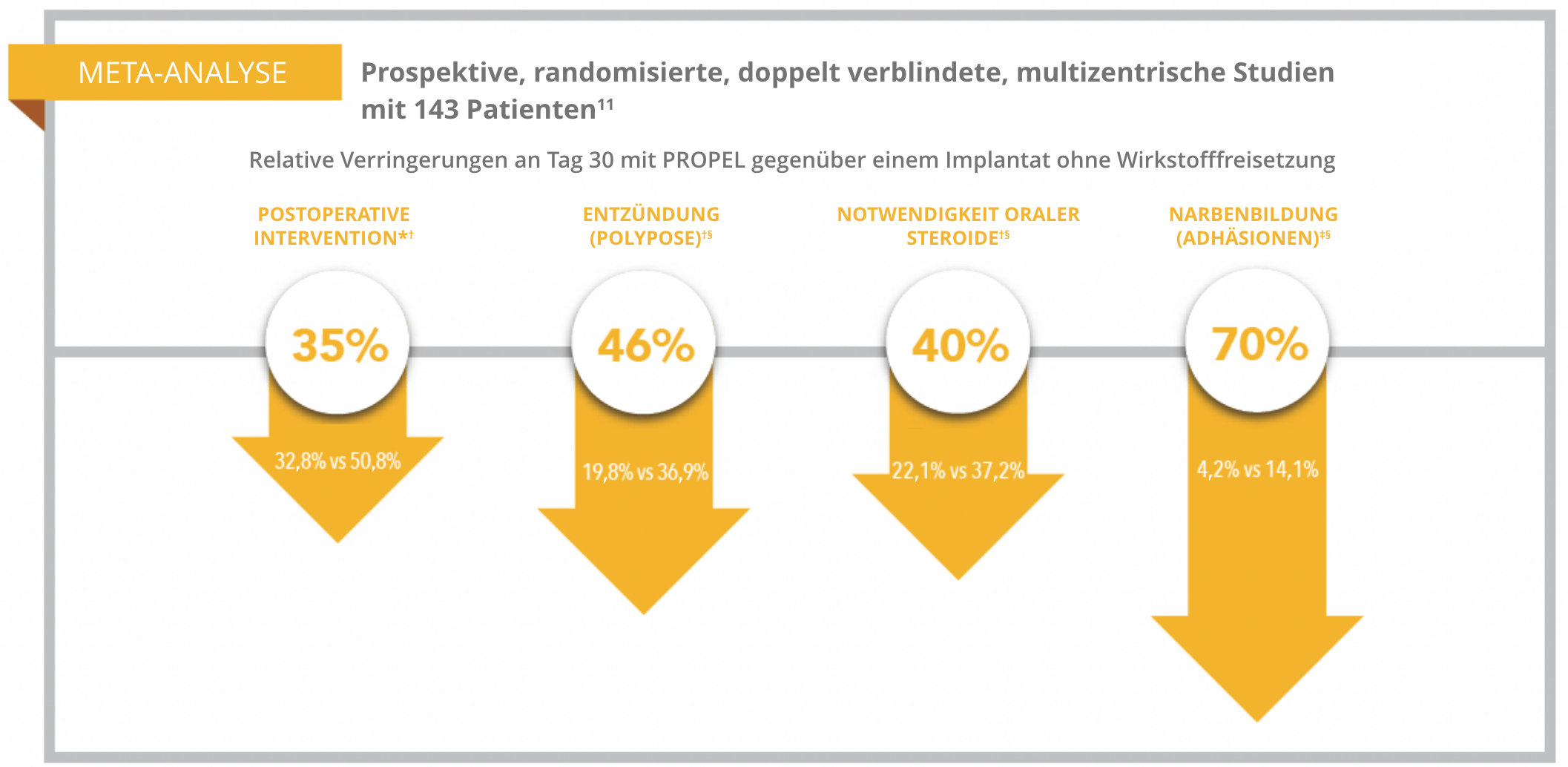
PROPEL-Studiendesign: Meta-Analyse von zwei prospektiven, randomisierten, doppelt verblindeten, multizentrischen Studien (Pilot und ADVANCE II), an denen 143 Patienten teilnahmen.
Gebrauchsanweisung (EU):
Patient Implant Information Leaflet (EU):
Literatur
- PROPEL [Gebrauchsanweisung]. Menlo Park, CA: Intersect ENT; 2014.
- PROPEL Mini [Gebrauchsanweisung]. Menlo Park, CA: Intersect ENT; 2016.
- PROPEL Contour [Gebrauchsanweisung]. Menlo Park, CA: Intersect END; 2021.
- Food and Drug Administration. Approval Order. https://www.access-data.fda.gov/cdrh_docs/pdf10/P1000445018A.pdf. Accessed June 24, 2019.
- Li PM, Downie D, Hwang PH. Controlled steroid delivery via bioabsorbable stent: safety and performance in a rabbit model. Am J Rhinol Allergy.2009;23(6):591-596.
- Lemke T, Williams D, Roche V, Zito SW, eds. Foye’s Principles of Medicinal Chemistry. 6th ed. Balitmore, MD: Lippincott Williams & Wilkins; 2008.
- Winkler J, Hochhaus G, Derendorf H. How the lung handles drugs: pharmacokinetics and pharmacodynamics of inhaled corticosteroids. Proc Am Thorac Soc. 2004;1(4):356-363.
- Sastre J, Mosges R. Local and systemic safety of intranasal corticosteroids. J Invenstig Allergol Clin Immunol. 2012:22(1):1-12.
- PubChem. Dexamethasone. https://pubchem.ncbi.nlm.nih.gov/compound/Dexamethasone. Accessed June 24, 2019.
- Hochhaus G. Pharmacokinetic/pharmacodynamic profile of mometasone furoate nasal spray: potential effects on clinical safety and efficacy. Clin Ther. 2008:30(1):1-13.
- Han JK, Marple BF, Smith TL, et al. Effect of steroid-releasing sinus implants on postoperative medical and surgical interventions: an efficacy meta-analysis. Int Forum Allergy Rhinol. 2012;2(4):271-279.
- Luong A, Ow RA, Singh A, et al. Safety and effectiveness of a bioabsorbable steroid-releasing implant for the paranasal sinus ostia: a randomized clinical trial. JAMA Otolaryngol Head Neck Surg. 2018;144(1):28-35.
- PROGRESS CSR, P500-0514, R28020, Rev 4.0, 28 December 2016.
- Murr AH, Smith TL, Hwang PH, et al. Safety and efficacy of a novel bioabsorbable, steroid-eluting sinus stent. Int Forum Allergy Rhinol. 2011;1(1):23–32.